Una base fuerte es la que se disocia completamente en el agua, es decir, aporta el máximo número de iones OH−. El ejemplo anterior, hidróxido potásico, es de una base fuerte.
Una base débil también aporta iones OH− al medio, pero está en equilibrio el número de moléculas disociadas con las que no lo están.
En este caso, el hidróxido de aluminio está en equilibrio (descomponiéndose y formándose) con los iones que genera.
Formación
igual es:
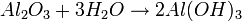
- Nomenclatura
Para crear una base usando diversas nomenclaturas para ellas tomadas a partir de los nombres de los elementos y juntándolos con un ion hidroxilo (OH), tomando el número de valencia del elemento y combinarlos (cambiándolos de posición) como se muestra en la tabla:
| Fórmula | Tradicional | Stock | IUPAC |
|---|---|---|---|
| Cu(OH) | Hidróxido cuproso | Hidróxido de cobre (I) | Monohidróxido de cobre |
| Cu(OH)2 | Hidróxido cúprico | Hidróxido de cobre (II) | Dihidróxido de cobre |
Cuando un elemento tiene más de dos valencias no se le pone nomenclatura tradicional. Al usar la menor valencia, el elemento termina en oso y cuando se usa la mayor termina enico. En la nomenclatura IUPAC se le va a dar una conformación de prefijos al elemento según su valencia usada (Mono, Di, Tri, Tetra, Penta, Hexa, etc) junto con la terminación -hidroxiu -oxidrilo que es el ion OH con carga −1.
By: Wikipedia


